تاريخ استفاده از مس حداقل به 10000 سال پيش ميرسد. در طول
دورهي ماقبل تاريخ كالكوليتيك Chalcolithic انسان دريافت كه
چگونه مس را استخراج كند و از آن تزئينات و ابزارآلات بسازد
(www.icsg.org). ابزارآلات مسي كشفشده قدمتي در حدود 5000 سال
پيش از ميلاد مسيح را نشان ميدهند (www.usgs.gov). مشاهدات
باستانشناسي نشانميدهد كه قدمت استفاده از مس بهعنوان
وسيلهاي زينتي در غرب آسيا مربوط به ده هزار سال قبل ميباشد.
آويزهي مسي متعلق به سال 8700 قبل از ميلاد يكي از قديميترين
موارد مصرف مس در زيورآلات است كه در شمال عراق کنوني پيدا شده
است (minerals.er.usgs.gov). در يکي از اهرام مصر يک سيستم
لولهکشي با مس پيدا شده که مربوط به5000 سال پيش است. مرد يخي
Oetzi، که در اروپا به دقت نگهداري ميشود و متعلق به3200 سال
قبل از ميلاد است، تبري با نوک مسي در دست دارد که درجه خلوص
فلز آن 7/99% ميباشد. مس به خاطر زيبايي درخشانش در باستان
براي ساخت آئينه استفاده ميشده است (www.icsg.org).
از مهمترين حوادث تاريخي تعيينكننده در مسير تكامل دانش بشر
در زمينهي استفاده از مس، كشف چگونگي توليد آلياژ برنز
ميباشد.
اكتشافات باستانشناسي نشان ميدهد كه در ايران از هزارهي
پنجم پيش از ميلاد، استفاده از مس رونق داشته است. اشياي مفرغي
به دست آمده از هزارههاي بعد، گوياي پيشرفت استفاده از مس
ميباشد.
وجود مس به صورت طبيعي و ويژگي مطلوب سهولت شكلپذيري يا
چكشخواري اين فلز با ابزار ابتدائي كه امكان ساخت ابزار
صنعتي، زيورآلات، لوله و مخازن آب، سكه، شمشير، مجسمه و مانند
آن را در دوران باستان فراهم مينمود، اين فلز را به صورت
مهمترين ماده در توسعهي تمدن بشر درآورد. مدارك موجود نشان
ميدهد، تا اواخر سالهاي 1800 ميلادي كاربرد مس بهطور نسبي
محدود بوده است. با اختراع داينامو، تلگراف، تلفن، برق و خطوط
انتقال نيرو در اواخر قرن نوزدهم، سيم به يك محصول نهايي بسيار
با اهميت تبديل شد و فلز مس به عنوان يك هادي صنعتي مهم از
توجه بسيار برخوردار شد (www.icsg.org).
اكتشافات و اختراعات مرتبط با برق و مغناطيس در اواخر قرن
هجدهم و اوايل قرن نوزدهم كه توسط دانشمنداني چون آمپر، فارادي
و اهم صورت گرفت، و محصولات ساخته شده از مس به آغاز انقلاب
صنعتي و سوقدادن مس به عصري جديد كمك كرد (www.icsg.org).
از اواخر قرن نوزدهم در اثر ارتباطي كه فلز مس با الكتريسته
پيدا نمود، هم كاربرد اين فلز از تنوع بسيار برخوردار گرديد و
هم بهدليل ارتباط مصرف الكتريسته با سطح زندگي مقدار مصرف مس
به يكي از شاخصهاي تعيين سطح زندگي در جوامع مختلف جهان مبدل
شد. اگرچه در قرن اخير مس، به عنوان دومين فلز پرمصرف، پس از
فولاد، مكان خود را به فلز آلومينيم واگذار نموده و به سومين
فلز تنزل يافته است، با اين وجود مس و آلياژهاي آن در بسياري
از كاربردهايي كه طي دوراني طولاني، شاخص آنها است، كماكان
بيرقيب مانده است. بهطور كلي در مواردي كه خواص انتقال
الكتريكي و حرارتي زياد با طول عمر و مقاومت قابل توجه نسبت به
فرسودگي مورد نياز است، مس و آلياژهاي آن كاربرد دارند. اين
كاربردها مرهون حداقل چهار ويژگي فيزيكي ـ شيميايي برتر مس است
كه به تنهايي و يا به صورت مجموع در انتخاب اين فلز نقش دارد.
مس در ميان فلزاتي كه كاربردهاي وسيع صنعتي دارند، هاديترين
فلز هم از نظر هدايت الكتريكي و هم انتقال حرارتي است و
نزديكترين فلز هادي به مس، آلومينيم است كه از نظر الكتريكي
كمي بيش از نصف و از نظر حرارتي نصف مس، خاصيت هادي بودن را
دارد.
ثبات شيميايي مس و تشكيل سريع غشاء نازكي از اكسيد بر سطح آن،
چنان مقاومتي نسبت به زنگزدگي و آلودگيهاي بيولوژيك در آن
ايجاد ميكند كه از نظر كار در آب و بخصوص آب شور دريا، هيچ
فلز يا آلياژ ديگري نميتواند با آن رقابت كند. سهولت كاربرد،
يكي ديگر از ويژگيهاي مهم مس و آلياژهاي آن است. مس و
آلياژهاي آن در صورتهاي مناسب به خوبي كشيده شده و به ورق
تبديل ميشوند. مس ضمن آنكه از خاصيت نرمي و شكلپذيري خوبي
برخوردار است، قابل آلياژ شدن با درجات مختلف سختي ميباشد.
ويژگيهاي مذكور آنچنان دامنه وسيعي از كاربرد براي مس و
آلياژهاي آن ايجاد كرده است كه در كليهي ماشينآلات و تجهيزات
صنعتي و خانگي، وسايل حمل و نقل، صنايع نظامي به نوعي حضور
يافته و مقدار مصرف آن طي كمتر از يك قرن در حدود 20 برابر
افزايش يافته است (فرشچي منفرد، 1374).
بيش از 70% مس توليدشدهي جهان در صنعت الكتريسيته و الكترونيك
مورد استفاده قرار ميگيرد. علاوه بر اين مس در كشاورزي و
زيستشناسي كاربرد فراواني دارد. مس يكي از تشكيلدهندههاي
همهي بافتهاي زيستي است كه براي رشد عادي و مناسب گياهان و
جانوران نياز است. نبود آن مضر بوده و مقدار كم آن براي سلامتي
انسان لازم است كه اين مقدار از طريق آب و غذا جذب بدن ميشود.
مس و تركيبات آن مانند فلزات ديگر (جيوه و سرب) خطرناك نبوده و
تاكنون هيچ نوع بيماري در اثر مس از انسانهايي كه ساليان دراز
با مس و تركيبات آن كار ميكنند، گزارش نشده است. در عوض گاهي
گفته ميشود كه بعضي از مردم سالمتر شده و در برابر
سرماخوردگي و ديگر بيماريها مقاومت پيداكردهاند. تاريخ
استفاده از تركيبات مس به 4000 سال قبل از ميلاد مسيح
برميگردد، جايي كه در آن مصريان از سولفات مس به عنوان
نگهدارنده، در فرآيند رنگسازي استفاده ميكردند. امروزه بعد
از گذشت 6000 سال سولفات مس هنوز هم در صنعت رنگ كاربرد دارد.
كاربرد ديگر تركيبات مس در قديم براي ساختن پمادهاي دارويي
بوده است. 400 سال قبل از ميلاد، يونانيان سولفات مس را در
درمان بيماريهاي ريوي تجويز ميكردند. در قرن 18 اين ماده
كاربرد وسيعي در پزشكي، براي مداواي نارساييهاي ذهني و ريوي،
نزد پزشكان دنياي غرب پيدا كرد. جالب اينجاست كه سولفات مس
هيچكدام از اثرات خود را در طي قرنها از دست نداده و هيچ نوع
ضرري از آن گزارش نشده است. اين تركيب در حال حاضر نيز در
قبايل بدوي آفريقا براي درمان بيماريهاي پوستي استفاده
ميشود. كاربرد ديگر مس بهعنوان عامل ضد انگلهاي زيستي مانند
قارچ و حشرات است. از سال 1838 سولفات مس براي حفظ الوارهاي
چوب استفاده ميشد و هم اكنون نيز جزء مواد اصلي نگهدارندههاي
چوب است.
80 سال پيش مشخص شد كه بسياري از جلبكها در برابر مس بسيار
حساسند، بنابراين نمكهاي مس توسط مهندسين آب براي جلوگيري از
گسترش جلبكها در ذخيرههاي آبي مورد استفاده قرار گرفت. كمتر
از ppm 2 مس در آب ميتواند بيماريهايي كه توسط كرمهاي آبزي
(مانند كرم شيستوزوما در كشورهاي استوايي) منتقل ميشود را
كنترل كند (www.icsg.org).
برخي ديگر از كاربردهاي مس عبارتند از:
1. سيمهاي مسي.
2. لولههاي مسي.
3. دستگيرههاي درب و ساير وسايل منزل.
4. مجسمهسازي، مثلاً مجسمه آزادي در ايلات متحده شامل 81194.4
كيلوگرم مس ميباشد.
5. آهنرباهاي الکتريکي.
6. موتورها، بخصوص موتورهاي الکترومغناطيسي.
7. موتور بخار وات.
8. کليدها و تقويتکنندههاي الکتريکي.
9. لامپهاي خلاء، لامپهاي پرتوي کاتدي ومگنترونهاي اجاقهاي
مايکروويو.
10. هدايتکنندهي موج براي تشعشع مايکروويو.
11. به علت خاصيت هدايت بهتر آن نسبت به آلومينيم، کاربرد مس
در ICها به جاي آلومينيم روبه افزايش است.
12. بهعنوان جزئي از سکهها.
13. در ساخت ظروف و وسايل آشپزي، از جمله ماهيتابه.
14. بيشتر سرويسهاي قاشق چنگال (flatware) قاشقها،چنگالها و
چاقوهاي نقره نيکلي داراي مقاديري مس هستند.
15. اگر نقرهي استرلينگ در ظروف غذاخوري بکار رفته باشد،
حتماً بايد داراي درصد کمي مس باشد.
16. بهعنوان بخشي از لعاب سراميکي و در رنگآميزي شيشه.
17. مالاكيت کربنات مس سبزرنگي است که بهوسيله آن ظاهر منحصر
به فرد بامها يا گنبدهاي با پوشش مس روي بعضي ساختمانها
ساخته ميشود.
18. وسايل موسيقي، بهخصوص سازهاي بادي و سازهاي سيمي.
19. بهعنوان يک بيواستاتيک در بيمارستانها و پوشاندن
قسمتهاي مختلف کشتي براي حفاظت در برابر بارناکلها و
ماسلها.
20. سولفات مس به عنوان سم كشاورزي و تصفيهكنندهي آب مورد
استفاده قرار ميگيرد.
21. تركيبات مس نظير محلول فلينگ بهطور گستردهاي در تجزيهي
شيميايي و آزمايش كردن شكر به كار ميروند.
مصارف برقي مس:
صنعت برق يكي از بزرگترين مصرفكنندگان مس است زيرا مس بهترين
فلز ارزان براي انتقال برق است، همچنين مس در مقايسه با ساير
انتقالدهندهها از استاندارد خاصي برخوردار است
(www.icsg.org).
علاوه براين، قدرت استثنايي مس، انعطاف پذيرياش و مقاومتاش
در برابر وادادگي و خوردگي، آن را به ارجحترين و ايمنترين
انتقالدهنده براي ساخت سيم تبديل كرده است.
مس همچنين در كابلهاي برق، به صورت عايقبندي شده يا نشده، و
براي كاربردهاي ولتاژ پايين، متوسط يا بالا مورد استفاده قرار
ميگيرد.
ICSG با مشاركت ICA، IIEC و CFC1 در حال حاضر از پروژهاي براي
افزايش استفاده از محصولات تشديدكنندهي مسي و كارآمد از نظر
انرژي در چين و هند حمايت ميكنند. معرفي و ارتقاء چنين
فنآوريهايي به بهبود بازدهي انرژي، كاهش اثرات مخرب گازهاي
گلخانهاي و افزايش استاندارهاي زندگي در نواحي روستايي منجر
خواهد شد. مس بخش اصلي موتورها و تبديلكنندههاي كارآمد است.
الكترونيك و ارتباطات:
كاربرد فيبر نوري در خطوط اصلي ارتباطات به انقلابي در صنعت
ارتباطات از راه دور منجر شده است. عليرغم كنار گذاشتن مس در
بخشي از نظام توزيع، نياز به مس در اجتماعاتي كه با سيم به هم
متصل ميشوند افزايش يافته است. مس هنوز انتقالدهندهي مناسبي
براي بخشهاي انتهايي مسير انتقال است. همچنين خطوط اشتراك
داخلي، شبكههاي محلي، كامپيوترهاي شخصي و ساير سختافزارها
همگي به مس و آلياژهاي آن، بخصوص اتصالدهندهها نيازمندند.
فنآوري XDSL (خط اشتراكدهندهي ديجيتالي) به زيرساختهاي مسي
و موجود سيمهاي تلفن معمولي اين امكان را ميدهد تا اطلاعات
را با سرعت بالا انتقال دهند. اين فنآوري براي كاربران
اينترنت به معناي اتصال به 5/1 بيت در ثانيه به جاي 56 هزار
بيت در ثانيه است.
سازندگان نيمههاديها اخيراً چيپ مسي جنجالبرانگيزي ارائه
كردهاند. با استفاده از مس در مدار چيپهاي سيليكوني،
ريزپردازندهها اين توانايي را مييابند تا با استفاده از
انرژي كمتر در سرعتهاي بالاتري عمل كنند.
ساختمان و عمارت:
مقاومت بامهاي مسي علاوه بر جذابيتشان در برابر شرايط هوايي
سخت بسيار معروف است. در اكثر ساختمانهاي عمومي، ساختمانهاي
تجاري و خانهها از مس براي مقاومت در برابر آب باران و
بامسازي استفاده ميشود.
برق جلاي سبز رنگ و تاثيرگذاري كه نماي كلاسيكي از گرمي و
زيبندگي به مس اعطا ميكند، حاصل آب و هواي طبيعي است.
سيستمهاي آبرساني و گرمايي مسي مشخصهاي از ايمني ارزشمند در
ساختمانهاست.
مس و برنج موادي هستند كه در لولهكشي، شيرهاي آب، سوپاپها و
وسايل منزل به كار ميروند.
مس برخلاف لوله پلاستيكي نميسوزد، ذوب نميشود يا در صورت
بروز آتش گازهاي سمي يا زيانآور آزاد نميكند. لولههاي مس
همچنين از سيستمهاي آبرساني در برابر باكتريهاي مرگبار مثل
ليجيونلا legionella محافظت ميكند.
استفاده از دستگيرهها و بشقابهاي مسي متضمن استفاده از خواص
زيستثباتي مس و ممانعت از انتقال بيماري و ميكروب است.
حمل و نقل:
كليه اشكال اصلي حمل و نقل براي اجراي نقشهاي حياتيشان به مس
وابستهاند. از آلياژهاي مس-نيكل بر روي بدنههاي قايقها و
كشتيها براي كاهش پوسيدگي ناشي از آب دريا استفاده ميشود و
بدين طريق مقدار آبنشيني كشتيها كاسته شده و مصرف سوخت بهبود
مييابد.
موتورها، سيمكشي، رادياتورها، اتصالدهندهها، ترمزها و
ياتاقانها: امروزه در هر خودرو بهطور ميانگين در حدود 6/27
كيلوگرم مس و در يك بوئينگ 400-747، 4000 كيلوگرم مس به كار
ميرود.
هدايت گرمايي برتر مس، قدرت، مقاومت در برابر خوردگي و قابليت
بازيافت مس، آن را به فلزي مناسب براي رادياتورهاي خودكار و
كاميون مبدل كرده است.
فنآوريهاي توليد جديد فرآيندها و طراحيهاي ابداعي، نفوذ مس
را در بازار رادياتور بيشتر خواهد كرد چون كه رادياتورهاي جديد
مسي سبكتر، كوچكتر و كارآمدتر هستند.
لوازم و ماشينآلات صنعتي:
هر جا كه لوازم و ماشينآلات صنعتي باشد، بهتر است كه مس و
آلياژهاي آن هم حضور داشته باشند. آلياژهاي مس بخاطر دوام،
قابليت ماشيني و توانايياش براي انعطافپذيري و دقت بالا براي
ساخت محصولاتي نظير دندهها، ياتاقانها و تيغههاي توربين
مناسباند.
قابليتها و تواناييهاي فراوان مس براي انتقال گرما و مقاومت
در محيطهاي سخت آن را به انتخابي مناسب براي تجهيزات تبادل
گرما، لولههاي فشار و خمرهها تبديل كرده است.
خواص مقاومت در برابر خوردگي مس و آلياژهاي مس( نظير برنج،
برنز و مس- نيكل) آنها را بخصوص براي استفاده در دريا و ساير
محيطهاي مورد نياز مناسب كرده است.
ظروف، مخازن، لولههايي كه در معرض آب دريا هستند، پروانه
كشتيها، سكوهاي نفتي و ايستگاههاي برق ساحلي همگي به مقاومت
مس در برابر خوردگي نيازمندند.
مصرفكننده و محصولات عمومي:
مس از آغاز تمدن مورد استفاده جوامع مختلف براي ساخت سكه بوده
است. امروزه كشورها اسكناسهاي با ارزش كمتر را جايگزين
سكههاي مسي كردهاند چون دوام سكههاي مزبور 10، 20 و حتا 50
بار بيشتر است. سكههاي يورو كه در سال 2002 ارائه ميشوند،
حاوي مس خواهند بود. مس و فراوردههاي مسي در ادارات، خانهها
و كارگاهها مورد استفاده قرار ميگيرند. كامپيوترها، وسايل
الكتريكي، ظروفهاي تزييني ساخته شده از برنج و قفل و كليدها
برخي از محصولات عموميتري هستند كه در آنها از فوائد مس
استفاده شده است.
كشاورزان در نواحي از زمين خود كه مقدار مس آن كم است، از مس
براي تغذيه دام و محصول استفاده ميكنند. خواص غنيتر غذايي كه
اكثر آنها مورد نياز غذاي كودكان است، در مس يافت ميشود.
استفادههاي كشاورزي از تركيبات مس:
تركيبات مس كاربرد گستردهاي در كشاورزي دارند. در سال 1769
كشف شد كه بر روي دانهاي كه در محلول رقيقي از سولفات مس
خيسانده شود ديگر قارچ رشد نميكند. بزرگترين كشف در اين باره
در سال 1880 اتفاق افتاد. هنگاميكه دانشمندان فرانسوي در حال
جستجوي درماني براي بيماري Downy Mildew در درختان انگور منطقه
بودند، متوجه شدند كه اين درختان در اطراف بزرگراهها رشد
ميكنند. اين بزرگراهها، به سولفات مس مخلوط با آهك آغشته مي
شدند تا از چسبيدن دانههاي انگور، به پاي عابران، جلوگيري
كند. درختان انگوري كه در اين مناطق رشد ميكردند، به اين
بيماري دچار نميشدند. اين مشاهده سبب شد كه مخلوط سولفات مس و
آهك در سال 1885 به عنوان داروي ضد بيماري Downy Mildewشناخته
شود و هماكنون نيز مورد استفاده قرار ميگيرد. به مخلوط
سولفات مس و آهك در آب Bordeaux گفته ميشود. بعدها اين تركيب
(سولفات مس و كربنات كلسيم) به عنوان عامل ضد بيماريهاي قارچي
در گياهان مختلف شناخته شد و سالانه هزاران تن از آن توليد
ميگردد. علاوه بر اين نمكهاي مس به خاكهايي كه كمبود مس
دارند، اضافه ميشود. سولفات مس بخاطر خاصيت ضد قارچي و ضد
باكتريايي خود در كشاورزي، براي جلوگيري از فساد ذخاير و كنترل
بيماريهاي جانوري استفاده ميشود. سولفات مس يا سنگ آبي با
فرمول شيميايي CuSO35H2O بيشترين كاربرد را در بين نمكهاي مس
داراست. در حال حاضر بيش از 100 كارخانهي توليد سولفات مس
وجود دارد و سالانه 200000 تن از آن مصرف ميشود كه 4/3 آن در
كشاورزي مورد استفاده قرار ميگيرد.
نقش تركيبات مس در كشاورزي و ديگر صنايع :
نقش سولفات مس در كشاورزي را ميتوان بهطور زير خلاصه كرد:
1- تهية Bordeauxو Burgundy.
2- كنترل بيماريهاي قارچي.
3- جبران كمبود مس در خاك.
4- جبران كمبود مس در جانوران.
5- افزايش و تحريك رشد مرغهاي گوشتي.
6- عامل نابودي كرمها و حلزونها بويژه كرم كبد گوسفند.
كاربرد ديگر تركيبات مس:
- استات مس:
استات مس به عنوان عامل ضد قارچ بهصورت محلول 1 كيلوگرم در
500 ليتر آب استفاده ميشود. طرز تهيهي اين ماده از واكنش
اسيد استيك بر مس، اكسيد مس، كربنات مس و سولفات مس بدست
ميآيد. علاوه براين استات مس به عنوان كاتاليزور در بعضي
واكنشهاي زيستي، شيميايي مانند رنگآميزي پارچه و رنگآميزي
سراميك و غيره مورد استفاده واقع ميشود.
- اكسيد مس:
بهصورت الكتريكي از مس و يا از واكنش بازها با سولفات مس بدست
ميآيد. كاربرد آن بهعنوان عامل ضد قارچ و همچنين پوشانندهي
دانهها بوده و نيز در رنگآميزي شيشه و چيني استفاده ميشود.
علاوه براين براي جلوگيري از كثيف شدن تابلوهاي نقاشي و همچنين
در صنعت رايون كاربرد دارد.
- كلريد مس:
از انحلال اكسيد مس در اسيد كلريدريك يا واكنش با كلر بدست
ميآيد. كاربرد اصلي آن در صنعت نفت براي شيرينسازي نفت و
براي تجزيهي كاتاليزورها در فرآيندهاي شيميايي و همچنين
نگهدارنده در صنعت چاپ و رنگآميزي چيت است.
- اكسي كلريد مس:
از واكنش اسيد هيدروكلريد با مس يا اكسيداسيون محصولات
سوسپانسيوني كلريدي بدست ميآيد و كاربرد اصلي آن بهعنوان
عامل ضد قارچ است.
- نيترات مس:
از انحلال كربنات مس در اسيد نيتريك بدست آمده و در
سراميكسازي، آتشنشاني و عكاسي كاربرد دارد.
- سييانيد مس:
از واكنش سيانيد سديم و سولفات مس بدست ميآيد و در
الكتروپلاتينگ مس استفاده ميشود.
- نفتنات مس:
از واكنش سولفات مس و اسيد نفتنيك در تركيب با يك باز ويا با
گرم كردن اسيد نفتنيك حاصل شده و به عنوان نگهدارندهي چوب و
عامل گندزدا مورد استفاده قرار ميگيرد.
- صابون مس:
از واكنش متقابل صابون محلول و سولفات مس ساخته ميشود. مقدار
كمي از اين صابونها مانند استرات مس، اولئات مس و ابيتات مس
به عنوان عامل گندزدا مصرف ميشود و همچنين در روغنها مورد
استفاده دارند(www.copper.org).


 وجود
مس به صورت طبيعي و ويژگي مطلوب سهولت شکلپذيري يا چکشخواري اين فلز با
ابزار ابتدائي که امکان ساخت ابزار صنعتي، زيورآلات، لوله و مخازن آب،
سکه، شمشير، مجسمه و مانند آن را در دوران باستان فراهم مينمود، اين فلز
را به صورت مهمترين ماده در توسعهي تمدن بشر درآورد. مدارک موجود نشان
ميدهد، تا اواخر سالهاي 1800 ميلادي کاربرد مس بهطور نسبي محدود بوده
است. با اختراع داينامو، تلگراف، تلفن، برق و خطوط انتقال نيرو در اواخر
قرن نوزدهم، سيم به يک محصول نهايي بسيار با اهميت تبديل شد و فلز مس به
عنوان يک هادي صنعتي مهم از توجه بسيار برخوردار شد (www.icsg.org).
وجود
مس به صورت طبيعي و ويژگي مطلوب سهولت شکلپذيري يا چکشخواري اين فلز با
ابزار ابتدائي که امکان ساخت ابزار صنعتي، زيورآلات، لوله و مخازن آب،
سکه، شمشير، مجسمه و مانند آن را در دوران باستان فراهم مينمود، اين فلز
را به صورت مهمترين ماده در توسعهي تمدن بشر درآورد. مدارک موجود نشان
ميدهد، تا اواخر سالهاي 1800 ميلادي کاربرد مس بهطور نسبي محدود بوده
است. با اختراع داينامو، تلگراف، تلفن، برق و خطوط انتقال نيرو در اواخر
قرن نوزدهم، سيم به يک محصول نهايي بسيار با اهميت تبديل شد و فلز مس به
عنوان يک هادي صنعتي مهم از توجه بسيار برخوردار شد (www.icsg.org).











 گازی به اسید سولفوریک اضافه میشود، الئوم یا
گازی به اسید سولفوریک اضافه میشود، الئوم یا 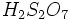 ایجاد میشود. واکنش اسید سولفوریک با آب بسیار
ایجاد میشود. واکنش اسید سولفوریک با آب بسیار 
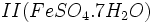 که
که 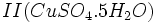 که
که 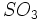 میگردد. ترکیب آب و
میگردد. ترکیب آب و 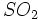 :
: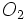 در دمای بالاتر از 450 درجه سانتیگراد و فشار 2atm و کاتالیزور پنتا اکسید وانادیم ، واکنش داده و
در دمای بالاتر از 450 درجه سانتیگراد و فشار 2atm و کاتالیزور پنتا اکسید وانادیم ، واکنش داده و 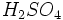 :
: این وبلاگ توسط دانشجوی ارشد شیمی پلیمر جهت ارائه جدید ترین مطالب در مورد شیمی راه اندازی شده است. امیدوارم بتوانم سهمی هرچند کوچک در گسترش این علم داشته باشم
این وبلاگ توسط دانشجوی ارشد شیمی پلیمر جهت ارائه جدید ترین مطالب در مورد شیمی راه اندازی شده است. امیدوارم بتوانم سهمی هرچند کوچک در گسترش این علم داشته باشم